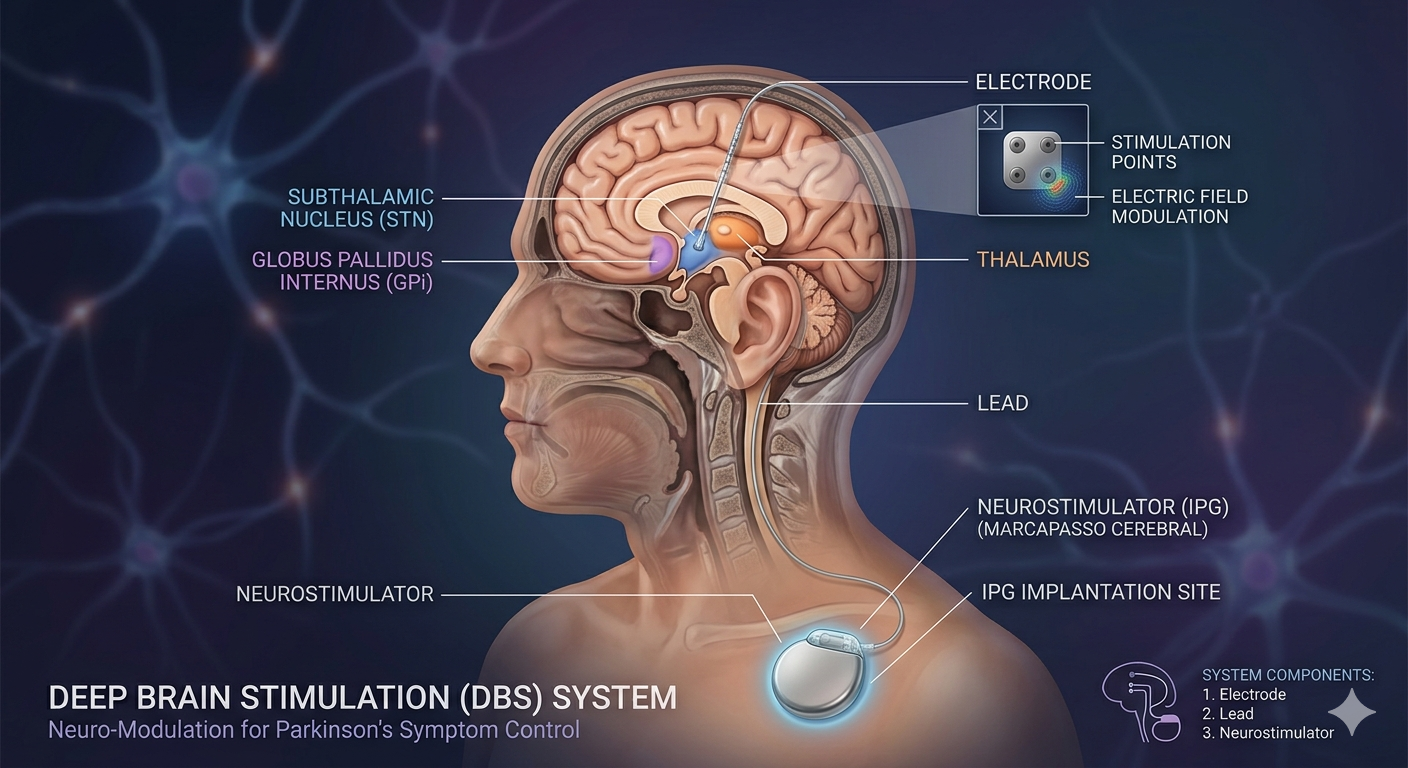
O encaminhamento oportuno para estimulação cerebral profunda (ECP) pode melhorar significativamente a vida de pessoas com doença de Parkinson (DP), tratando sintomas motores e não motores refratários ao tratamento medicamentoso. No entanto, estabelecer diretrizes uniformes de encaminhamento continua sendo um desafio devido à heterogeneidade dos sintomas da DP, à resposta variável de diferentes sintomas à estimulação, à evolução do perfil de risco-benefício da cirurgia conforme a doença progride e à disponibilidade de outras terapias assistidas por dispositivos. Apesar dessas complexidades, o encaminhamento oportuno e bem fundamentado é crucial para garantir que os candidatos adequados não sejam negligenciados. Estas recomendações de consenso de especialistas visam apoiar neurologistas e outros profissionais de saúde que encaminham pacientes, oferecendo uma estrutura prática que promova a consideração adequada e oportuna da ECP para cada paciente. O desenvolvimento de redes locais estruturadas, que conectem hospitais a provedores comunitários, pode aprimorar a comunicação e simplificar o processo de encaminhamento para candidatos à ECP. Dessa forma, podem ajudar a reduzir as barreiras ao tratamento, apoiar a tomada de decisão compartilhada e ampliar o acesso a essa intervenção segura, eficaz e transformadora.
Link para pesquisa em: https://pmc.ncbi.nlm.nih.gov/articles/PMC12848073/
Referência:
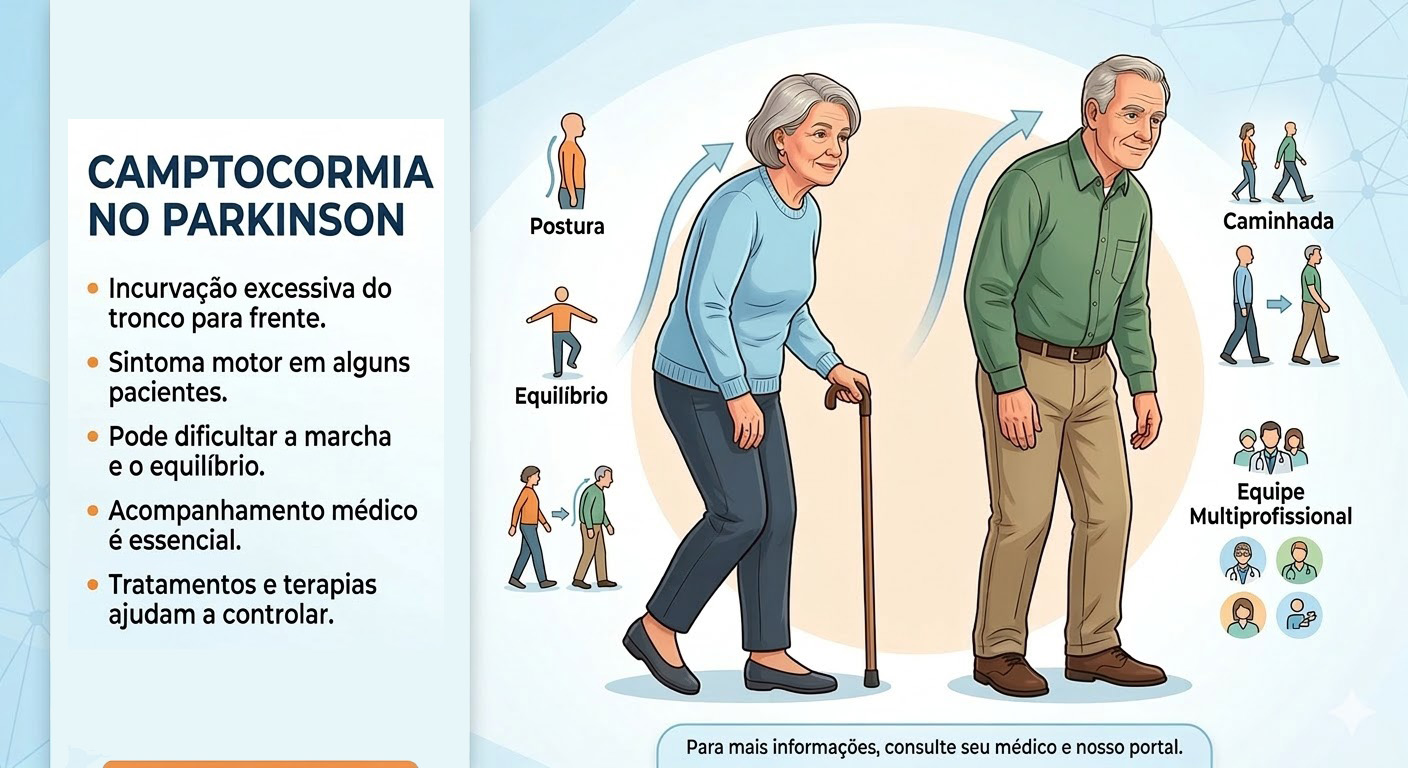
XU, J. et al. Physical Therapy and Exercise for Camptocormia in Parkinson’s Disease: A Systematic Review. PMC PubMed Central, 2024. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC12848073/. Acesso em: 13 mar. 2026.
Safarpour D, Spindler M, Turner TH, Patel N, Vaou O, Cabrera LY, Tolleson C, Tipton PW, Aquino C, Herrington TM, Sidiropoulos C, Hantke N, Lotia M, Miocinovic S, Sharma VD, Mills KA, Wyman-Chick K, Kilbane C, Luca C, Almeida L, Rosenow J, Ooi HY, Mari Z, Luo L, Munhoz RP, Jesus S, Sarva H, Arena M, Revuelta G, Chou KL, Fasano A, Siddiqui MS, Jimenez-Shahed J; Functional Neurosurgical working group of the Parkinson Study Group. Consensus expert recommendations for referral of Parkinson’s disease patients for deep brain stimulation surgery. NPJ Parkinsons Dis. 2026 Jan 3;12(1):30. doi: 10.1038/s41531-025-01241-3. PMID: 41484162; PMCID: PMC12848073.